免疫檢查點是完整T細胞功能所不可(kě)缺少的蛋白(bái),當人(rén)體(tǐ)需要阻止免疫功能時,這類蛋白(bái)會起到重要的抑制T細胞功能的作(zuò)用。目前已知的用于藥物的免疫檢查點包括PD1、CTLA4等。
一、PD1或PDL1單抗藥物的原理(lǐ)
PD1屬于T細胞的抑制信号的一種重要受體(tǐ),其配體(tǐ)(可(kě)以理(lǐ)解爲與之配套的結合上就(jiù)能啓動免疫抑制作(zuò)用的分(fēn)子)是PDL1。
PD1是完整T細胞功能所不可(kě)缺少的蛋白(bái),當人(rén)體(tǐ)需要阻止免疫功能時,PD1會起到重要的抑制T細胞功能的作(zuò)用。
狡猾的腫瘤利用了這一點,當T細胞來(lái)殺傷癌細胞的時候,癌細胞表面會動态表達PDL1,從(cóng)而讓T細胞“休眠”,從(cóng)而阻止并逃過T細胞的殺傷。
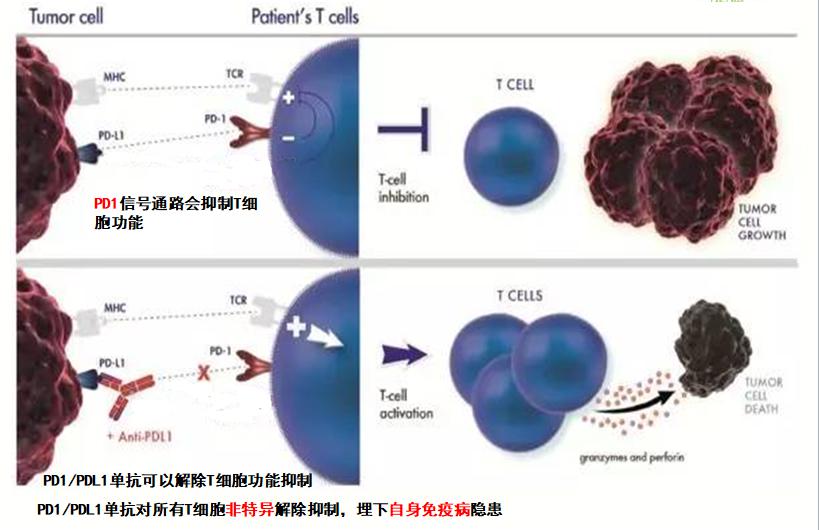
PD1或PDL1單抗藥物可(kě)以阻止腫瘤細胞的PDL1與T細胞的PD1結合,從(cóng)而解除T細胞的功能抑制,起到殺傷腫瘤的療效。
PD1/PDL1抗體(tǐ)藥物已成爲癌症治療的明星,跻身(shēn)于一線治療藥物行列。
2017年(nián)美國(guó)FDA甚至批準了一類PD1單抗藥物的不分(fēn)癌種的應用,隻需要腫瘤在基因上體(tǐ)現爲微衛星不穩定(MSI-H)或錯配修複蛋白(bái)缺陷(dMMR)即可(kě)。
2018年(nián)美國(guó)FDA批準了PD1單抗用于非小細胞肺癌的術(shù)後輔助防複發的應用。
目前已上市及待上市的PD1/PDL1單抗藥物:
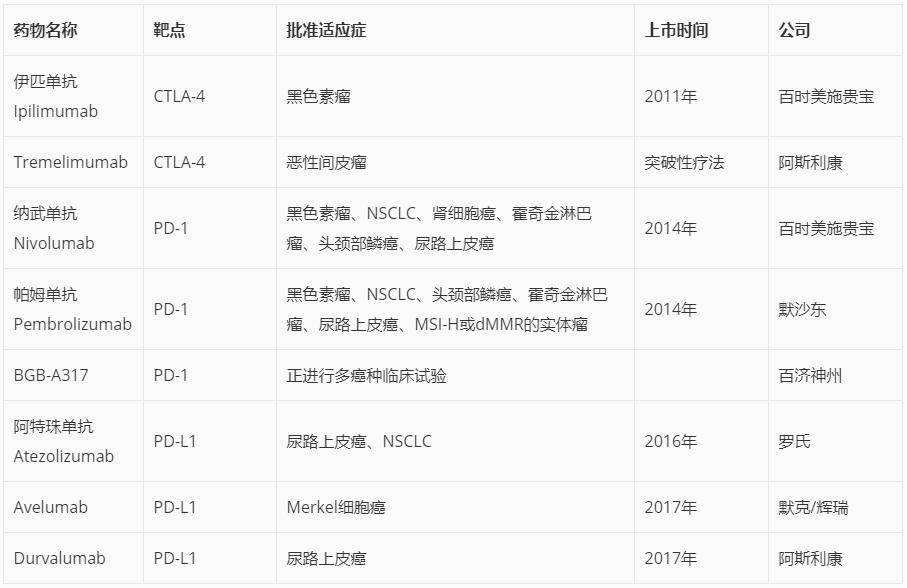
二、PD1/PDL1單抗最重要的用藥指征——TMB
由于戴上了數不清的“突破”光(guāng)環,因此很多“走投無路(lù)”的晚期癌症患者視PD-1免疫療法爲“救命稻草”。但(dàn)事(shì)實上,這種免疫療法并不是适合每一個人(rén),臨床試驗表明,隻有約20-40%的患者能夠從(cóng)中獲益。
換句話(huà)說(shuō),如(rú)果癌症患者“盲試”PD-1免疫療法,那麽可(kě)能會浪費金錢與時間。因此,實現精準免疫治療,選擇優勢獲益人(rén)群就(jiù)顯得(de)至關重要。
目前,從(cóng)關鍵臨床研究提供的數據來(lái)看(kàn),PD-L1的表達是否可(kě)以指導臨床用藥,選擇獲益人(rén)群,結論還(hái)不一緻。
随着研究的進一步深入,科(kē)學家們發現了更多的潛在的生(shēng)物标志物。包括腫瘤突變負荷(TMB)、微衛星高度不穩定(MSI-H)和錯配基因修複缺失(MMR)。其中,腫瘤突變負荷(TMB)作(zuò)爲一項新興的診斷方式,已經成功的引起了研究人(rén)員(yuán)的注意!
先前,百時美公布的一項代号爲CheckMate-032的試驗數據表明:
對于腫瘤突變負荷(TMB)高的患者來(lái)說(shuō):單藥使用PD-1抗體(tǐ)Opdivo (Nivolumab)的有效率21%,中位總生(shēng)存期爲5.4個月;聯合CTLA-4抗體(tǐ)Yervoy (Ipilimumab)的有效率爲46%,中位總生(shēng)存期高達22個月。
對于腫瘤突變負荷(TMB)低的患者來(lái)說(shuō):單藥使用PD-1抗體(tǐ)Opdivo (Nivolumab)的有效率5%,中位總生(shēng)存期爲3.1個月;聯合CTLA-4抗體(tǐ)Yervoy (Ipilimumab)的有效率爲16%,中位總生(shēng)存期僅有3.4個月。
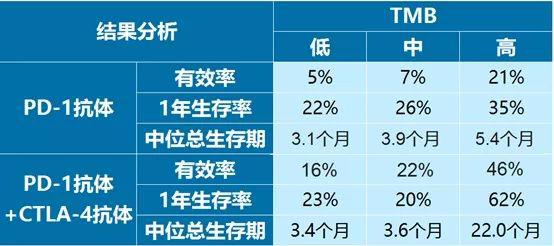
近日(rì),百時美公布了首個、也是目前唯一一個評估并證實無論PD-L1表達水平如(rú)何, I-O/I-O一線聯合治療能夠爲腫瘤突變負荷(TMB)高表達的患者帶來(lái)PFS顯著獲益的III期臨床研究數據。研究采用Foundation Medicine公司的分(fēn)析驗證方法FoundationOne CDx對TMB進行檢測。
令人(rén)驚喜的是,這項名代号爲“CheckMate-227”的III期臨床結果顯示:首次證實了在預先定義的腫瘤突變負荷(TMB)高表達的非小細胞肺癌患者中,Opdivo (Nivolumab)和Yervoy(Ipilimumab)聯合治療在PFS上表現出了顯著優越性。
表明腫瘤突變負荷(TMB)能夠作(zuò)爲一種重要且獨立的預測性生(shēng)物标志物,以鑒别出那些可(kě)能在Opdivo聯合Yervoy一線治療中獲益的NSCLC患者。
對此,百時美公司的董事(shì)長兼首席執行官Giovanni Caforio博士表示,CheckMate-227的數據是癌症研究中的重要突破,對于确定哪些患者能夠從(cóng)該聯合療法中獲益,邁出了極爲重要的一步。
而在此之前,JohnsHopkins Kimmel癌症中心的研究人(rén)員(yuán)也曾在《新英格蘭醫學雜志》上公開發文:表示“突變負荷”或腫瘤DNA中存在的突變數目是預測檢查點抑制劑的這類免疫療法針對不同癌症産生(shēng)反應的良好标志物,可(kě)以用來(lái)指導這類免疫療法的臨床試驗。
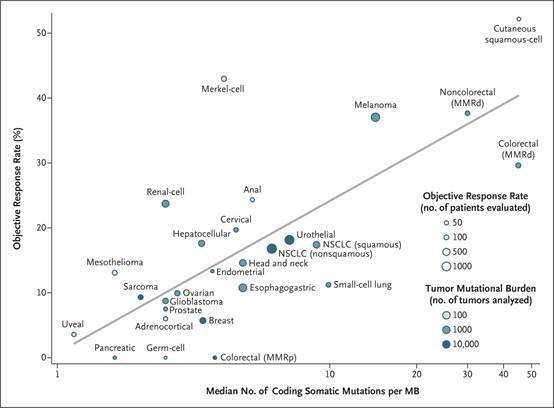
腫瘤突變負荷越高,癌症免疫治療藥物的成功率就(jiù)越高
過程中,研究人(rén)員(yuán)共同梳理(lǐ)了使用檢查點抑制劑治療多種不同類型癌症的臨床試驗結果的醫學文獻,并将這些發現與來(lái)自(zì)不同腫瘤類型的數千個腫瘤樣本的突變負荷數據結合起來(lái)。通過分(fēn)析27 個不同癌症類型,研究人(rén)員(yuán)發現了一種明顯的聯系:一種癌症類型的突變負荷越高,對檢查點抑制劑有反應的可(kě)能性就(jiù)越大(dà)。而且值得(de)注意的是,超過50%的癌症對于檢查點抑制劑的反應程度,均可(kě)由該癌症的突變負荷解釋。
也就(jiù)是說(shuō),腫瘤突變負荷越高,免疫治療的有效性也就(jiù)越好!這種說(shuō)法乍一聽似乎不太合理(lǐ)。但(dàn)腫瘤的基因突變越多,産生(shēng)的異常蛋白(bái)質就(jiù)可(kě)能也越多,因此就(jiù)有更大(dà)的可(kě)能性激活免疫系統。因此,直接測定腫瘤組織中的突變數量,也就(jiù)是所謂的腫瘤突變負荷,是可(kě)以預測PD-1抑制劑等免疫治療的療效的。(本節文字來(lái)源:醫麥客公衆号文章(zhāng))
三、免疫檢查點抑制劑的局限性
目前免疫檢查點抑制劑的總體(tǐ)響應率不高,隻有20~30%,高TMB的患者的療效會更好。
另外這類藥物把所有T細胞的免疫抑制都(dōu)解除了,并非所有T細胞都(dōu)是識别腫瘤的,有些T細胞是識别自(zì)身(shēn)正常細胞的,解除抑制之後會導緻這些T細胞攻擊自(zì)身(shēn)正常組織,引發自(zì)身(shēn)免疫病。
還(hái)有免疫檢查點抑制劑隻是恢複了天然T細胞的功能,能否克服腫瘤完全依賴于患者自(zì)身(shēn)免疫細胞的功能,但(dàn)患者自(zì)身(shēn)能識别腫瘤的T細胞的數量有限,而且T細胞和腸道菌群經過反複化療之後總體(tǐ)功能低下,都(dōu)會是限制這類藥物效果的因素。
因此這類藥物有效的人(rén)群大(dà)多體(tǐ)現出兩個特點,一是起效相(xiàng)對較慢(màn),而且需要長期用藥,這需要極高的經濟負擔;二是被化療破壞了腸道菌群的患者,效果會差;三是對這類藥物響應的患者,可(kě)以獲得(de)比較長的生(shēng)存期,這也充分(fēn)說(shuō)明免疫治療才是最終極的長效治療。